Theo đó, Cục Quản lý dược (Bộ Y tế) đã ra quyết định đình chỉ lưu hành và thu hồi nhiều loại sản phẩm không đáp ứng quy định trong tháng 10/2019.
Cụ thể, ngay từ đầu tháng 10, Cục Quản lý Dược có văn bản gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, các cơ sở nhập khẩu thuốc yêu cầu thu hồi các thuốc chứa Ranitidine do phát hiện chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư ở hàm lượng vượt quá ngưỡng cho phép của quốc tế.
Để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược yêu cầu thu hồi tất cả 11 loại thuốc thành phẩm có tên sau:
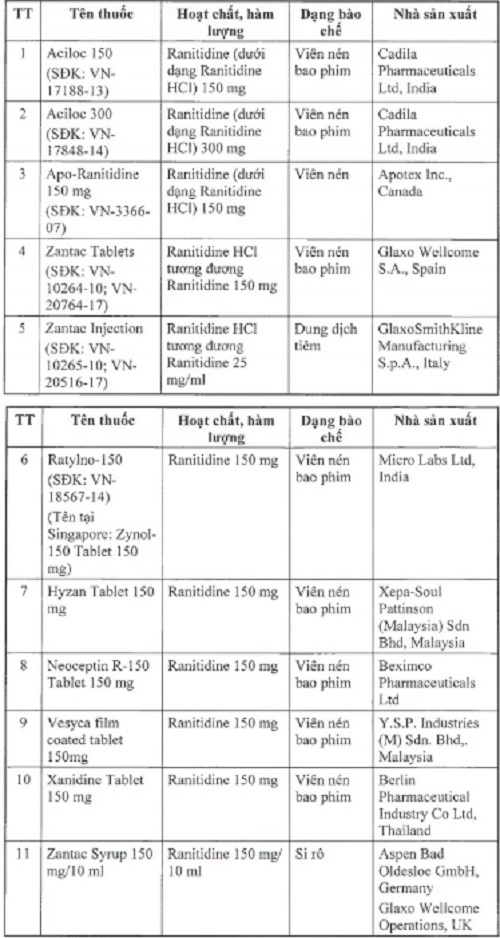 Danh sách 11 thuốc thành phẩm Cục quản lý dược yêu cầu thu hồi
Danh sách 11 thuốc thành phẩm Cục quản lý dược yêu cầu thu hồiTiếp đến ngày 11/10/2019 Cục Quản lý Dược ra thông báo thu hồi trên toàn quốc loại thuốc Viên nén Methylprednisolone 16mg, SĐK: VD-19224-13, Số lô: 804060; NSX: 20.04.2018, HD: 20.04.2021 do Công ty TNHH dược phẩm USA-NIC sản xuất do mẫu kiểm nghiệm cho thấy không đạt tiêu chuẩn chất lượng về chỉ tiêu hòa tan.
Thuốc Methylprednisolon 16mg thuộc nhóm thuốc hóc môn, nội tiết tố. Thuốc chỉ định dùng khi bất thường chức năng vỏ thượng thận; Viêm da dị ứng, viêm đường hô hấp dị ứng, viêm khớp, thấp khớp, bệnh về máu; Viêm khớp dạng thấp; Lupus ban đỏ, hen phế quản, viêm loét đại tràng, thiếu máu tan máu, giảm bạch cầu hạt. Bệnh dị ứng nặng bao gồm phản vệ; trong điều trị ung thư: leukemia cấp tính, u lympho, ung thư vú, ung thư tuyến tiền liệt; hội chứng thận hư nguyên phát.
Đình chỉ lưu hành, thu hồi thuốc nội tiết Methylprednisolone kém chất lượng.
Cục Quản lý Dược yêu cầu công ty TNHH dược phẩm USA-NIC phối họp với nhà phân phối thuốc, gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng Viên nén Methylprednisolone.
Cách đó không lâu 5 ngày sau khi Cục quản lý dược (Bộ Y tế) ra quyết định đình chỉ lưu hành, thu hồi thuốc nội tiết Methylprednisolone kém chất lượng. thì ngày Ngày 16/10, Cục Quản lý Dược cũng đã ra thông báo số 17610/QLD-CL về việc đình chỉ lưu hành thuốc viên nén bao phim AMK 625 không đạt tiêu chuẩn chất lượng.
Theo đó, Cục Quản lý Dược căn cứ vào các quy chế dược hiện hành của Việt Nam và công văn số 485/VKNTKHTH ngày 25/9/2019 của Viện kiểm nghiệm thuốc Tp. Hồ Chí Minh gửi kèm phiếu kiêm nghiệm số 1484/VKN-YC2019 và số 1485/VKN-YC2019 ngày 18/9/2019 báo cáo kết quả lấy mẫu bổ sung đối với lô thuốc viên nén bao phim AMK 625, số lô: 99R002, ngày SX: 09/4/2018, HD: 09/4/2020 nêu trên là không đạt tiêu chuẩn chất lượng về chỉ tiêu Độ hòa tan (Amoxicillin).
Ngày 23/10, Cục Quản lý Dược đã có văn bản đình chỉ lưu hành, thu hồi toàn quốc lô sản phẩm kem dưỡng trắng da 3 tác dụng sữa non ngọc trai do không đạt tiêu chuẩn chất lượng.
Cụ thể, sản phẩm bị đình chỉ lưu hành và thu hồi là sản phẩm kem dưỡng trắng da 3 tác dụng sữa non ngọc trai số lô: 030119; ngày sản xuất: 3/1/2019; hạn sử dụng: 3 năm kể từ ngày sản xuất; số tiếp nhận phiếu công bố sản phẩm mỹ phẩm: 002093/15/CBMP-HCM do Công ty TNHH Thương mại – Sản xuất – Xuất nhập khẩu mỹ phẩm Thịnh Phát sản xuất.
Thu hồi toàn quốc lô sản phẩm kem dưỡng trắng da 3 tác dụng sữa non ngọc trai do không đạt tiêu chuẩn chất lượng.
Đồng thời yêu cầu Công ty TNHH Thương mại – Sản xuất – Xuất nhập khẩu mỹ phẩm Thịnh Phát gửi thông báo thu hồi tới những nơi phân phối, sử dụng sản phẩm nêu trên và tiến hành thu hồi toàn bộ lô sản phẩm mỹ phẩm không đáp ứng quy định; gửi báo cáo thu hồi sản phẩm mỹ phẩm không đáp ứng quy định về Cục Quản lý Dược trước ngày 20/11/2019.
 | Chống gian lận thương mại hàng Trung Quốc gắn “made in Vietnam” con đường gian nan Sau loạt chuyện về việc hàng Trung Quốc được gắn “made in Vietnam” Trưa ngày 2/11 lô hàng của Công ty TNHH Cao su Talalay Việt Nam đã bị Chi cục Hải quan cửa khẩu Cảng Sài Gòn khu vực 1 phối hợp với Phòng Cảnh sát kinh tế PC03 - Công an TP.HCM Đội kiểm soát Hải quan và Biên phòng TP.HCM kiểm tra mở container 40 feet nhập từ Trung Quốc về Việt Nam |
Mới đây nhất, ngày 25/10 Cục Quản lý Dược vừa có văn bản yêu cầu thu hồi toàn quốc viên nang mềm Halaxamus không đạt tiêu chuẩn chất lượng về chỉ tiêu tính chất, định lượng, độ đồng đều khối lượng.
Cụ thể, căn cứ vào các quy chế dược hiện hành của Việt Nam và công văn số 112/TTKN-HCTH của Trung tâm kiểm nghiệm thuốc, mỹ phẩm, thực phẩm tỉnh Vĩnh Phúc, Cục Quản lý Dược đã ban hành công văn về việc xử lý lô thuốc viên nang mềm Halaxamus (Acetylcystein 200 mg), SĐK: VD-25911-16, số lô: 6880119; ngày SX: 11/6/2019; HD: 11/6/2022 do Chi nhánh Công ty cổ phần dược phẩm Phong Phú - Nhà máy sản xuất dược phẩm Usarichpharm (Lô số 12 Đường số 8, khu công nghiệp Tân Tạo, phường Tân Tạo A, quận Bình Tân, Tp. Hồ Chí Minh) sản xuất. Mẫu thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu tính chất, định lượng, độ đồng đều khối lượng./.
PV (T/H)