Cục Quản lý Dược (Bộ Y tế) ban hành Quyết định số 159 /QĐ-QLD về việc thu hồi giấy đăng ký lưu hành thuốc đối với thuốc đã được cấp giấy đăng ký lưu hành tại Việt Nam.
Theo đó, Cục Quản lý Dược- Bộ Y tế quyết định thu hồi giấy đăng ký lưu hành đối với thuốc Prednison 5mg đã được cấp giấy đăng ký lưu hành tại Việt Nam. Lý do thu hồi thuốc là do cơ sở đăng ký thuốc đề nghị tự nguyện thu hồi giấy đăng ký lưu hành thuốc tại Việt Nam.
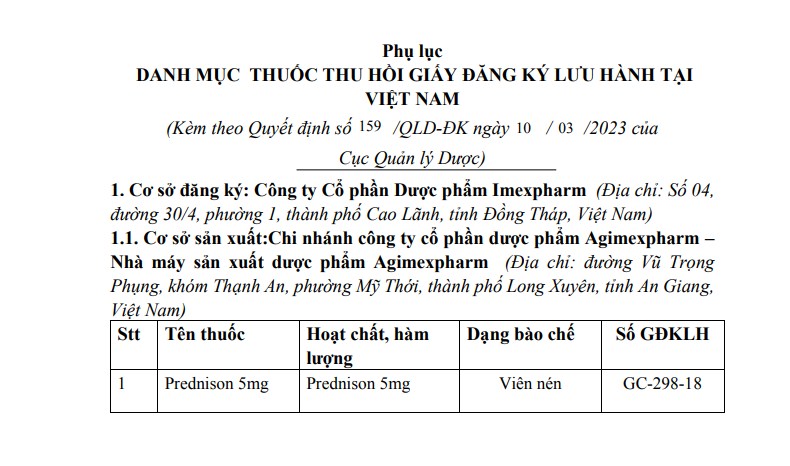 Thu hồi giấy đăng ký lưu hành đối với thuốc Prednison 5mg.
Thu hồi giấy đăng ký lưu hành đối với thuốc Prednison 5mg.
Quyết định cũng nêu rõ, thuốc được sản xuất trước ngày Quyết định này có hiệu lực được phép lưu hành đến hết hạn dùng của thuốc.
Cơ sở đăng ký, sản xuất thuốc có trách nhiệm theo dõi và chịu trách nhiệm về chất lượng, an toàn, hiệu quả của thuốc trong quá trình lưu hành. Quyết định này có hiệu lực kể từ ngày ký.
Trước đó, Cục Quản lý Dược- Bộ Y tế quyết định thu hồi giấy đăng ký lưu hành đối với 07 thuốc đã được cấp giấy đăng ký lưu hành tại Việt Nam, lý do các cơ sở đăng ký thuốc đề nghị tự nguyện thu hồi giấy đăng ký lưu hành thuốc tại Việt Nam, bao gồm:
Paracetamol RO 500mg (số đăng ký VD-28966- 18 và VD-28967- 18), cơ sở sản xuất: Công ty cổ phần dược phẩm Imexpharm (Địa chỉ: Số 4, đường 30/4, Phường 1, TP Cao Lãnh, Tỉnh Đồng Tháp, Việt Nam);
Ospexin 250mg, số đăng ký VD-28957- 18, cơ sở sản xuất: Chi nhánh 3 - Công ty cổ phần dược phẩm Imexpharm tại Bình Dương. (Địa chỉ: Số 22, đường số 2, KCN Việt Nam-Singapore II, Phường Hòa Phú, TP Thủ Dầu Một, tỉnh Bình Dương, Việt Nam);
Cozomat 10, số đăng ký VD-35821- 22, cơ sở sản xuất: Công ty cổ phần thương mại dược phẩm Quang Minh (Địa chỉ:4A Lò Lu, phường Trường Thạnh, quận 9, Thành phố Hồ Chí Minh, Việt Nam);
Clorpheniramin-T, số đăng ký VD-25070- 16, cơ sở sản xuất: Công ty cổ phần dược phẩm Phong Phú - Chi nhánh nhà máy Usarichpharm (Địa chỉ: Lô số 12, đường số 8, Khu công nghiệp Tân Tạo, phường Tân Tạo A, quận Bình Tân, Thành phố Hồ Chí Minh, Việt Nam);
SM. Risedronat, số đăng ký VD-35923- 22, cơ sở sản xuất: Công ty cổ phần dược phẩm Hà Tây (Địa chỉ: Tổ dân phố số 4, phường La Khê, quận Hà Đông, thành phố Hà Nội, Việt Nam);
Magne-B6 corbière, số đăng ký VD-32207- 19, cơ sở sản xuất: Công ty cổ phần Sanofi Việt Nam (Địa chỉ: Lô I-8-2, đường D8, Khu công nghệ cao, phường Long Thạnh Mỹ, thành phố Thủ Đức, Thành phố Hồ Chí Minh, Việt Nam).
Quyết định cũng nêu rõ, thuốc được sản xuất trước ngày Quyết định này có hiệu lực được phép lưu hành đến hết hạn dùng của thuốc.
Cơ sở đăng ký, sản xuất thuốc có trách nhiệm theo dõi và chịu trách nhiệm về chất lượng, an toàn, hiệu quả của thuốc trong quá trình lưu hành. Quyết định này có hiệu lực kể từ ngày ký.
Hoàng Hậu